| 职权编号 |
1421039 |
清单事项种类 |
其他职权类 |
| 职权名称 |
1431001 Y第一类医疗器械产品(变更信息、取消)备案 |
| 实施机构 |
行政事项服务科 |
| 受理地点 |
新乡市红旗区新二街360号行政服务中心二楼食药监局窗口 |
| 设立依据 |
| 1 |
【行政法规】《医疗器械监督管理条例》(国务院令第650号通过,2014年2月12日修订通过,2014年6月1日施行)
第八条 第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。
第十条第一款 第一类医疗器械产品备案,由备案人向所在地设区的市级人民政府食品药品监督管理部门提交备案资料。其中,产品检验报告可以是备案人的自检报告;临床评价资料不包括临床试验报告,可以是通过文献、同类产品临床使用获得的数据证明该医疗器械安全、有效的资料。
第十条第三款 备案资料载明的事项发生变化的,应当向原备案部门变更备案。 |
| 2 |
【部门规章】《医疗器械注册管理办法》(食品药品监督管理总局令第4号,2014年6月27日审议通过,2014年10月1日起施行)
第五十七条 第一类医疗器械生产前,应当办理产品备案。
第五十九条 已备案的医疗器械,备案信息表中登载内容及备案的产品技术要求发生变化的,备案人应当提交变化情况的说明及相关证明文件,向原备案部门提出变更备案信息。备案资料符合形式要求的,食品药品监督管理部门应当将变更情况登载于变更信息中,将备案资料存档。
第六十条 已备案的医疗器械管理类别调整的,备案人应当主动向食品药品监督管理部门提出取消原备案;管理类别调整为第二类或者第三类医疗器械的,按照本办法规定申请注册。 |
|
| 收费依据及标准 |
不收费 |
| 各环节责任事项及责任科室 |
|
受理
|
1.受理责任(即办):公示依法应当受理提交的材料;一次性告知补证材料;依法受理或不予受理(不予受理应当告知理由)。
|
行政事项服务科
|
|
形式审查
|
2.形式审查责任(2个工作日):对申请材料依法进行形式审核,提出审核意见。
|
行政事项服务科
|
|
出具备案凭证
|
3.出具备案凭证责任(2个工作日):予以备案的出具备案凭证,不予备案的告知理由。
|
行政事项服务科
|
|
送达
|
4.送达责任(1个工作日):送达备案凭证,并公开信息。
|
行政事项服务科
|
|
事后监管
|
5.事后监管责任:依法监督检查。
|
行政事项服务科
|
|
|
6.其他法律规范规定应履行的责任。
|
行政事项服务科
|
|
| 服务电话及监督电话 |
| 编号 |
联系电话 |
| 1 |
监督电话 |
0373-6389396 |
| 2 |
服务电话 |
0373-3076956 |
|
| 救济途径(复议、诉讼) |
自知道该具体行政行为之日起60日内向同级人民政府或上级主管部门申请行政复议,或6个月内直接向人民法院提起诉讼。
|
| 办事流程图 |
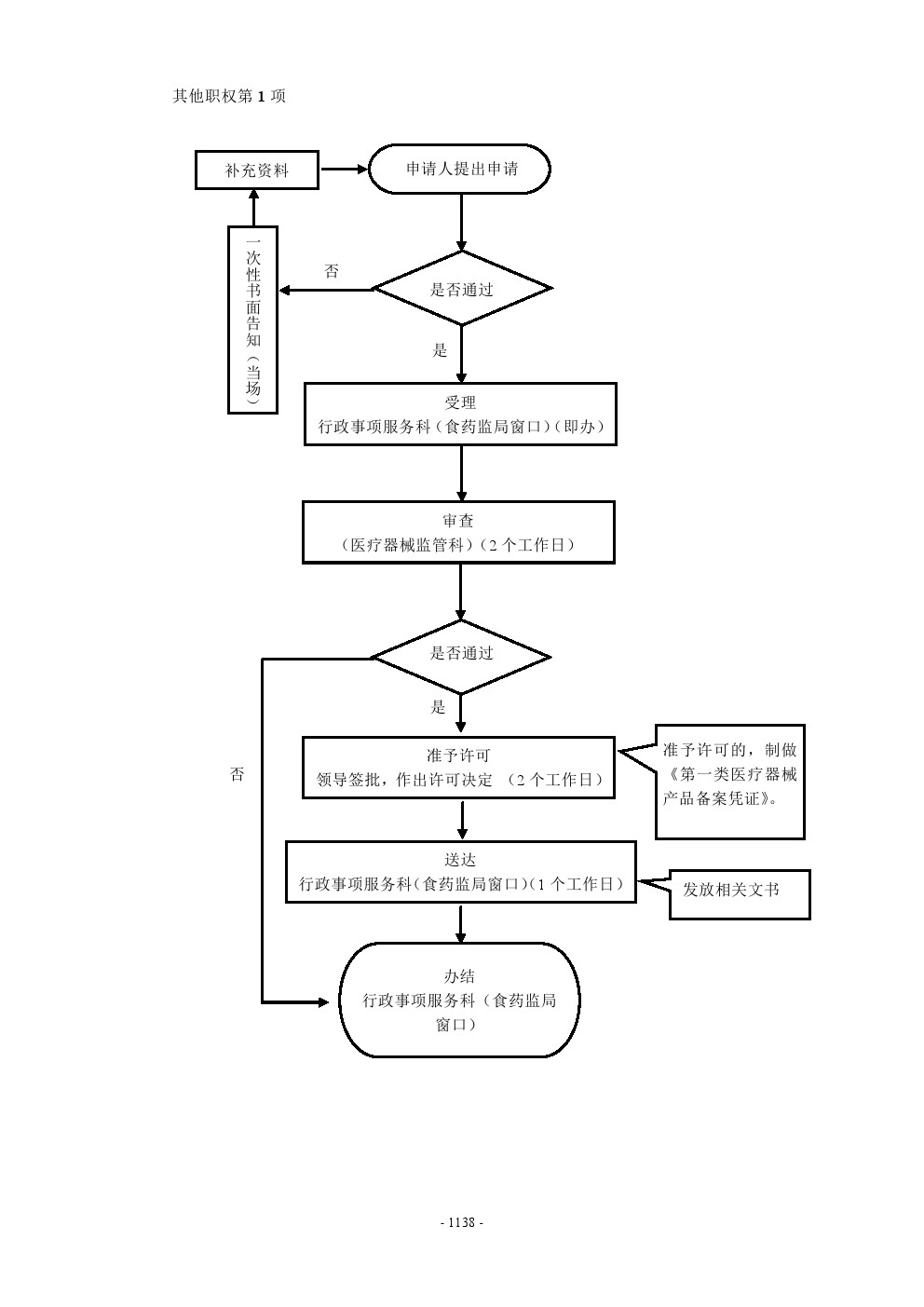 |
| 附件下载 |
|
无下载信息
|
